- Tác giả Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:46.
- Sửa đổi lần cuối 2025-01-23 12:52.
Pha loãng là quá trình làm cho dung dịch đậm đặc loãng hơn. Có nhiều lý do khiến ai đó có thể muốn pha loãng, từ những lý do nghiêm trọng đến đơn giản. Ví dụ, các nhà hóa sinh học pha loãng các dung dịch từ dạng cô đặc của chúng để tạo ra các dung dịch mới để sử dụng trong các thí nghiệm, trong khi mặt khác, những người pha chế thường pha loãng rượu với nước ngọt hoặc nước trái cây để làm cho cocktail ngon hơn. Công thức chung để tính độ pha loãng là NS1V1 = C2V2, với C1 và C2 đại diện cho nồng độ ban đầu và nồng độ cuối cùng của dung dịch, và V1 và V2 đại diện cho khối lượng.
Bươc chân
Phương pháp 1/2: Pha loãng chính xác các chất cô đặc thông qua phương trình pha loãng

Bước 1. Xác định những gì bạn biết và không biết
Pha loãng trong hóa học thường có nghĩa là lấy một lượng nhỏ dung dịch mà bạn biết nồng độ, sau đó thêm chất lỏng trung tính (chẳng hạn như nước) để tạo ra dung dịch mới có thể tích lớn hơn nhưng nồng độ thấp hơn. Điều này rất thường được thực hiện trong các phòng thí nghiệm hóa học, bởi vì, vì mục đích hiệu quả, thuốc thử thường được bảo quản ở nồng độ rất cao, sau đó được pha loãng để sử dụng trong các thí nghiệm. Thông thường, trong hầu hết các tình huống thực tế, bạn sẽ biết nồng độ của dung dịch ban đầu và nồng độ hoặc thể tích bạn muốn nồng độ cuối cùng của mình, nhưng không biết thể tích dung dịch ban đầu bạn cần để có được dung dịch cuối cùng.
- Tuy nhiên, trong các tình huống khác (đặc biệt là trong các bài toán ở trường), bạn có thể cần tìm các mảnh ghép khác - ví dụ: bạn có thể được cung cấp một thể tích và nồng độ ban đầu, sau đó được yêu cầu tìm nồng độ cuối cùng nếu bạn pha loãng dung dịch. đến âm lượng mong muốn. Trong bất kỳ trường hợp pha loãng nào, điều hữu ích là lưu ý các biến số đã biết và chưa biết trước khi bắt đầu.
-
Hãy kết thúc các câu hỏi ví dụ. Giả sử chúng ta được yêu cầu pha loãng dung dịch 5 M với nước để tạo thành 1 L dung dịch 1. mM. Trong trường hợp này, chúng ta biết nồng độ của dung dịch ban đầu và thể tích cũng như nồng độ cuối cùng mà chúng ta muốn, nhưng không biết lượng dung dịch ban đầu mà chúng ta cần thêm với nước để đạt được kết quả mong muốn.
Nhắc nhở: Trong hóa học, M là một đơn vị đo nồng độ được gọi là Molarity, biểu thị số mol của một chất trong một lít
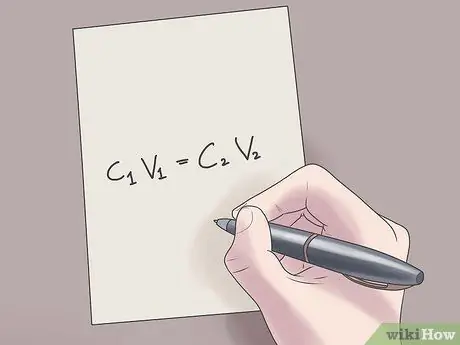
Bước 2. Cắm các giá trị của bạn vào công thức C1V1 = C2V2.
Trong công thức này, C1 là nồng độ ban đầu của dung dịch, V1 là thể tích của dung dịch ban đầu, C2 là nồng độ cuối cùng của dung dịch, và V2 là thể tích của dung dịch cuối cùng. Việc cắm các giá trị đã biết vào phương trình này sẽ giúp bạn tìm các giá trị chưa biết với ít khó khăn hơn.
- Bạn có thể thấy hữu ích khi đặt dấu chấm hỏi trước đơn vị bạn muốn tìm kiếm để giúp bạn giải quyết vấn đề đó.
-
Hãy tiếp tục ví dụ của chúng tôi. Chúng tôi sẽ nhập các giá trị mà chúng tôi biết như sau:
- NS1V1 = C2V2
- (5 triệu) V1 = (1 mM) (1 L). Hai nồng độ của chúng tôi có đơn vị khác nhau. Chúng ta hãy dừng lại ở đây và chuyển sang bước tiếp theo.

Bước 3. Xem xét bất kỳ sự khác biệt đơn vị nào
Vì các giải pháp liên quan đến sự thay đổi nồng độ (đôi khi có thể khá lớn), không có gì lạ khi hai biến trong phương trình của bạn có các đơn vị khác nhau. Mặc dù điều này dễ bị bỏ qua, nhưng các đơn vị không bằng nhau trong phương trình của bạn có thể khiến câu trả lời của bạn không chính xác. Trước khi kết thúc, chuyển đổi tất cả các giá trị với các đơn vị nồng độ và / hoặc thể tích khác nhau.
-
Trong ví dụ của chúng tôi, chúng tôi sử dụng các đơn vị khác nhau cho nồng độ của M (mol) và mM (milimolar). Hãy thay đổi số đo thứ hai của chúng tôi thành M:
- 1 mM × 1 M / 1.000 mM
- = 0,001 triệu

Bước 4. Kết thúc
Khi tất cả các đơn vị đều bằng nhau, hãy giải phương trình của bạn. Điều này hầu như luôn luôn có thể được thực hiện với đại số đơn giản.
-
Chúng tôi dừng vấn đề ví dụ của chúng tôi ở đây: (5 M) V1 = (1 mM) (1 L). Hãy tìm giá trị của V1 với đơn vị mới của chúng tôi.
- (5 triệu) V1 = (0,001 M) (1 L)
- V1 = (0,001 M) (1 L) / (5 M).
-
V1 = 0,0002 L, hoặc 0,2 mL.

Bước 5. Hiểu cách sử dụng câu trả lời của bạn một cách chính xác
Giả sử bạn đã tìm thấy giá trị còn thiếu của mình, nhưng bạn không chắc chắn cách sử dụng thông tin mới này trong độ pha loãng thực tế mà bạn cần làm. Điều này có thể hiểu được - ngôn ngữ của toán học và khoa học đôi khi không khớp với thế giới thực. Khi bạn biết bốn giá trị trong phương trình C1V1 = C2V2, pha loãng như sau:
- Đo thể tích V1 từ một dung dịch có nồng độ C1. Sau đó, thêm đủ chất pha loãng (nước, v.v.) để có tổng thể tích V2. Dung dịch mới này sẽ có nồng độ bạn muốn (C2).
- Ví dụ, trong ví dụ của chúng tôi, đầu tiên chúng tôi đo 0,2 mL dung dịch 5 M. Tiếp theo, chúng tôi sẽ thêm đủ nước để tăng thể tích của dung dịch lên 1 L: 1 L - 0,0002 L = 0,9998 L, hoặc 999,8 mL. Nói cách khác, chúng tôi sẽ thêm 999,8 mL nước vào dung dịch mẫu nhỏ của chúng tôi. Dung dịch pha loãng mới của chúng tôi có nồng độ 1 mM, là nồng độ mong muốn của chúng tôi.
Phương pháp 2 trên 2: Tạo dung dịch pha loãng đơn giản và thiết thực

Bước 1. Đọc bất kỳ bao bì để biết thông tin
Có nhiều lý do khiến bạn có thể muốn tạo dung dịch pha loãng ở nhà, trong bếp hoặc trong một phòng thí nghiệm không dùng hóa chất khác. Ví dụ, làm nước cam từ một cô đặc đơn giản là một sự pha loãng. Trong nhiều trường hợp, sản phẩm cần pha loãng có ghi thông tin về độ pha loãng cần pha ở đâu đó trên bao bì. Họ có thể có hướng dẫn chính xác để làm theo. Dưới đây là một số điều cần lưu ý khi tìm kiếm thông tin:
- Khối lượng sản phẩm đã sử dụng
- Khối lượng chất pha loãng đã sử dụng
- Loại chất pha loãng được sử dụng (thường là nước)
- Hướng dẫn pha trộn đặc biệt
- Bạn có thể không thấy thông tin về nồng độ chính xác của chất lỏng được sử dụng. Thông tin này không hữu ích cho người tiêu dùng bình thường.

Bước 2. Cho chất đóng vai trò là chất pha loãng vào dung dịch đậm đặc
Đối với các dung dịch pha loãng đơn giản trong gia đình, như pha loãng trong nhà bếp, bạn thực sự chỉ cần biết khối lượng cô đặc bạn đang sử dụng và nồng độ cuối cùng gần đúng mà bạn muốn trước khi bắt đầu. Pha loãng dịch cô đặc với một lượng chất pha loãng thích hợp, được xác định tùy thuộc vào thể tích của cô đặc ban đầu được sử dụng. Xem bên dưới:
- Ví dụ: nếu chúng ta muốn pha loãng 1 cốc nước cam cô đặc thành 1/4 nồng độ ban đầu, chúng ta sẽ thêm 3 chén nước vào cô đặc. Hỗn hợp cuối cùng của chúng ta sẽ có 1 cốc cô đặc trong 4 cốc toàn chất lỏng - 1/4 so với nồng độ ban đầu.
- Đây là một ví dụ phức tạp hơn: Nếu chúng tôi muốn pha loãng 2/3 cốc cô đặc thành 1/4 nồng độ ban đầu của nó, chúng tôi sẽ thêm 2 cốc nước, vì 2/3 cốc bằng 1/4 lần 2 & 2/3 cốc toàn bộ chất lỏng.
- Đảm bảo thêm chất của bạn vào một hộp đựng đủ lớn để chứa thể tích cuối cùng mà bạn muốn - một chiếc bát lớn hoặc hộp đựng tương tự.

Bước 3. Bỏ qua khối lượng bột trong hầu hết các trường hợp
Thêm bột (chẳng hạn như hỗn hợp đồ uống nhất định) vào chất lỏng thường không được coi là pha loãng. Sự thay đổi thể tích do thêm một lượng nhỏ bột vào chất lỏng thường đủ nhỏ đến mức không đáng kể. Nói cách khác, khi thêm một lượng nhỏ bột vào chất lỏng, chỉ cần thêm bột vào thể tích chất lỏng cuối cùng mong muốn của bạn và trộn.
Cảnh báo
- Tuân theo bất kỳ nguyên tắc an toàn nào do nhà sản xuất cung cấp hoặc công ty của bạn yêu cầu. Điều này đặc biệt quan trọng nếu bạn phải pha loãng dung dịch axit.
- Làm việc với các dung dịch có tính axit có thể yêu cầu các biện pháp và hướng dẫn an toàn chi tiết hơn so với các dung dịch không có tính axit.






